Contents
Muse細胞を用いた神経疾患新規治療の開発
脳血管疾患は、日本人の死因で常に上位であり、寝たきりとなる原因の第1位となっており、解決しなければならない大きな問題となっています。その脳血管疾患の中で最も患者数が多いのが、脳梗塞です。一度脳梗塞に陥ってしまうと、超急性期の血栓溶解療法・血栓回収療法のみが根本的な治療となるため、急性期を過ぎてしまうと基本的には脳梗塞の再発予防という治療しかありません。神経学的所見を改善させていくのは、本人のリハビリテーションのみというのが現状です。機能を失った梗塞巣を救出するために注目されているのが幹細胞治療で、現在数多くの幹細胞治療が研究されています。当科でもMuse細胞という細胞を用いて脳梗塞の幹細胞治療の研究を行っています。
Muse細胞 (Multilineage-differentiating Stress Enduring cells) は、 2010 年に東北⼤学の出澤真理教授のグループによって発⾒されました。体内で様々な種類の細胞に分化することができる多能性という特徴と腫瘍化が起こりにくい非腫瘍性という特徴を持ち合わせています。Muse 細胞はもともと体内に持ち合わせている内因性の修復幹細胞であるため、遺伝⼦の導⼊や分化誘導などの必要がなく、そのまま静脈内に投与するだけで損傷部位に集積・⽣着して組織を修復するという特徴を有しています。
具体的な研究内容としては、脳梗塞モデル動物に対してMuse細胞を投与し、神経症状の改善の評価や組織学的・分子細胞生物学的な評価を行っています。神経症状の改善を認める動物に、「なぜよくなったのか」、「どうすればより高い効果を得られるのか」を考え、研究しています。現在の脳梗塞治療に変革を起こす幹細胞治療を目指し、日々探求しています。
研究が進み、臨床の場に進めていく準備も整ってきたため、2018年から2021年にかけて実際にMuse細胞の製剤で患者さんを治療する「治験」を行いました。結果は論文にまとめている最中ですが、脳梗塞の患者さんに対して、広くこの治療が行えるようになるよう、努力を続けています。
新規脳梗塞治療薬SMTPの開発
以前から株式会社ティムスと協力し、SMTP化合物というユニークな化合物群の研究を行っています。血栓溶解作用・抗炎症作用などを併せ持つ特徴的な物質です。これらの作用から、血栓溶解薬でありながら、出血や脳浮腫(脳の腫れ)を抑えることが期待され、高い安全性と治療効果が得らえられる可能性があります。我々は、動物実験から研究を行い、現在は臨床にまで橋渡ししつつあります。
現在、基礎研究の大半を終え、tPAが適応にならない、12時間以内の脳梗塞などを主に対象として、多施設共同での第二相治験を行い、本薬剤を用いて治療した患者さんがプラセボ(偽薬)群と比較して、神経学的転帰が良好であることが示されました。本薬剤が脳梗塞患者の治療薬として承認されることを目指しています。
頭蓋骨再生材料の開発
医工学研究科骨再生医工学分野 鎌倉慎二教授、ならびに歯学系研究科の先生方との共同実験で、「スポンジで骨を作る」ともいうべき新規骨再生材料OCP/Colを脳疾患に応用する研究を行っています。臨床現場で使用できるようになるように、臨床研究/治験に進むことを目標にしています。
数値流体力学を用いた脳動脈瘤等の解析
もともとは工学技術である数値流体力学(CFD)を人体での解析に応用しています。流体科学研究所から教わり研究をはじめ、現在では自分たちでも計算を行っています。脳動脈瘤や頚動脈狭窄、脳動静脈奇形など、脳の血管が関係する様々な疾患の解析をし、予後を判断したり、治療シミュレーションを行ったりしています。
脳虚血後の分子シグナリング研究
脳虚血後のアポトーシスやフェロトーシスなどの分子シグナルや、最近では虚血後に誘導されるtRNAの変化などの詳細を検証し、新規治療開発の糸口をつかむ研究をしています。最近では、RNA修飾や今まであまり着目されてこなかったtRNAのシグナリングについても活発に研究を行っています。
また、いろいろな動物モデルには利点・欠点などがあるため、より良いモデルの開発なども継続して行っています。
新規医療機器開発
東北大学は医療機器開発が盛んであることを生かし、AIを組み込んだ医療機器開発などを行っていますが、詳細は割愛します。
高速イメージング技術による不均一細胞集団の網羅的な画像解析
腫瘍や血液などの生体組織は、さまざまな種類・性質・状態の細胞で構成されています。そのため、生体組織の特性をより深く理解するには、これらの不均一な細胞集団を網羅的に解析することが不可欠です。しかし、従来の顕微鏡やフローサイトメトリーなどの測定技術では、多様な細胞集団を詳細かつ統計的に解析することは困難でした。
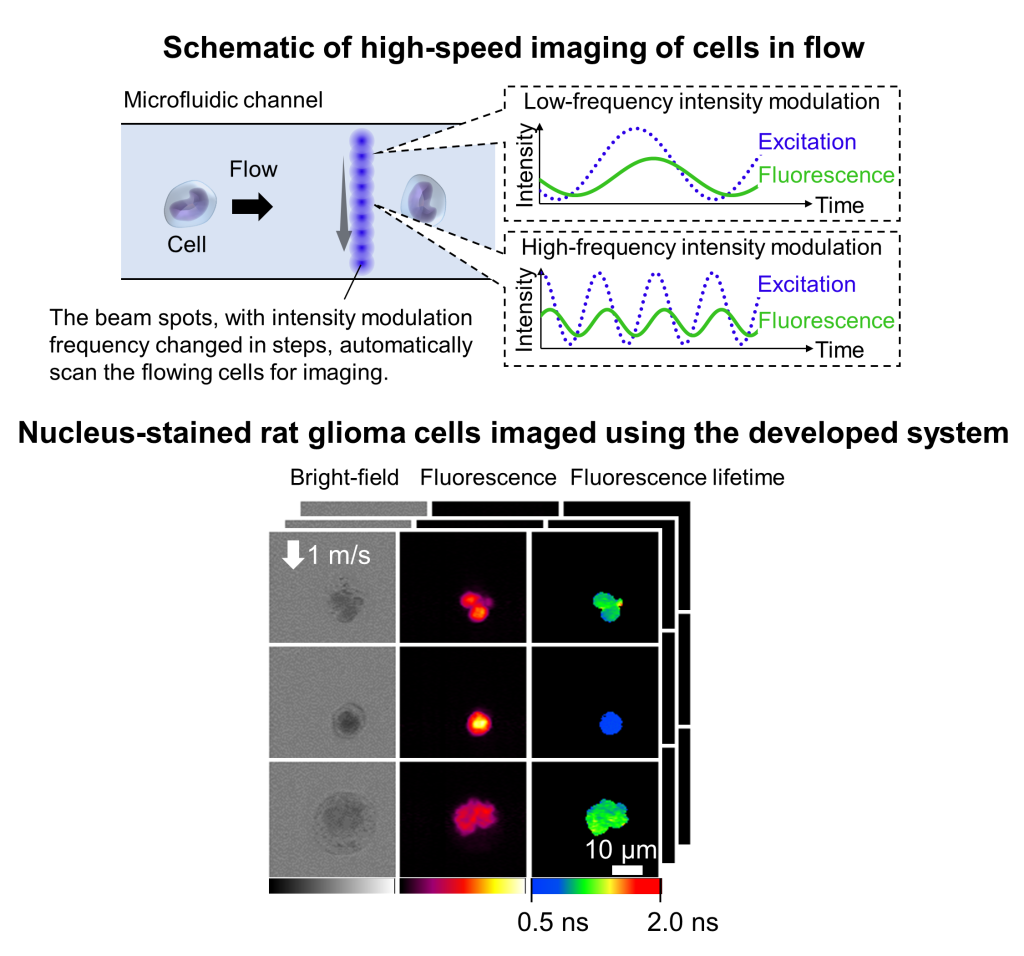
そこで当研究室では、細胞観察のための高速イメージング技術の開発を行い、不均一な細胞集団の網羅的な画像解析へと繋げています。具体的には、下図に示すように、微小な流路中にビームスポットを一列に並べ、複数の空間点を同時に計測することで、流れる細胞を一つ一つ高速に撮影することを可能にしています(1秒間に10,000細胞以上の画像取得が可能!)。各ビームスポットは異なる周波数で強度変調されているため、信号の一括検出後、信号処理技術により各信号を分離・復元することが可能です。これまでにこの技術を用いて、血液細胞や腫瘍細胞の解析を行っており、新型コロナウイルス感染症における血栓症の研究などにも貢献しています(M. Nishikawa, H. Kanno, Y. Zhou et al., Nature Communications 2021)。近年では、蛍光発光の寿命時間(蛍光寿命)を測定できる世界最高速の顕微鏡を開発し、イメージングの細胞解析能力を高めるとともに、生物医学への応用を進めています(H. Kanno et al., Nature Communications 2024)。蛍光寿命顕微鏡については、プレスリリースもご参照ください。